Forschung, die ans Herz geht
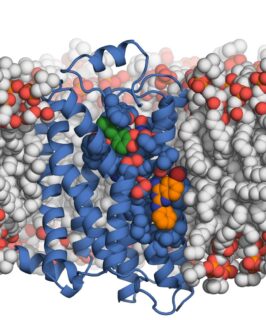
Neue Erkenntnisse zur zellulären Bindestelle von Adrenalin
Das von der Deutschen Forschungsgesellschaft geförderte Graduiertenkolleg „Medizinische Chemie selektiver GPCR-Liganden“ am Lehrstuhl für Pharmazeutische Chemie der FAU von Prof. Dr. Peter Gmeiner ist an einer internationalen Forschungsgruppe beteiligt, das G-Protein-gekoppelte Rezeptoren (GPCRs) untersucht. Jetzt gibt es neue Erkenntnisse zu allosterischen Modulatoren, die in Nature Chemical Biology veröffentlicht wurden (doi: 10.1038/s41589-020-0549-2).
Dabei handelt es sich, kurz gesagt, um Proteine in der Zellmembran, die Informationen von außen ins Innere der Zell transportieren. Die Bindestellen – orthosterische Bindungstaschen genannt – sind der Angriffspunkt für ungefähr 30 Prozent aller zugelassenen Arzneistoffe. Allerdings sind sich viele Rezeptoren ziemlich ähnlich, was es erschwert, selektive Medikamente zu entwickeln.
„Hier kommt nun ein von uns neu entdeckter negativer allosterischer Modulator ins Spiel. Die Kristallstruktur des β2-Adrenozeptors in Komplex mit dem Modulator zeigt eine neue Bindestelle auf der Außenseite des Rezeptors auf Höhe der Zellmembran“, erklärt Professor Gmeiner. „Auch dort können Wirkstoffe andocken. Im konkreten Fall ist das der Modulator AS408, der etwa zur Behandlung von Bluthochdruck, Herzrhythmusstörungen und Herzinsuffizienz zum Einsatz kommen könnte.“
Sind Struktur und Funktionsweise dieses Modulators bekannt, können entsprechende Arzneimittel passgenau entwickelt werden. Genau damit beschäftigt sich das Graduiertenkolleg an der FAU und die Arbeitsgruppe von Prof. Gmeiner, die bereits die Synthese, Strukturoptimierung und Teile der funktionellen Charakterisierung der potentiellen Modulatoren sowie Molekulardynamiksimulationen durchgeführt hat.
Hauptautor der Studie an der FAU ist Jonas Kaindl. Die von ihm durchgeführten Molekulardynamiksimulationen halfen beim genauen Verständnis der Wechselwirkungen des Rezeptors mit dem Modulator und bei der Aufklärung von dessen Wirkmechanismus. Zu den Kooperationspartnern der Erlanger Forschungsgruppe gehören unter anderem der Nobelpreisträger im Fach Chemie, Prof. Brian Kobilka, Stanford University, Prof. Brian Shoichet, University of California San Francisco, und Prof. Roger Sunahara, University of California San Diego.
Onlinezugriff unter nature.com/articles/s41589-020-0549-2
Weitere Informationen:
Prof. Dr. Peter Gmeiner
Lehrstuhl für Pharmazeutische Chemie
Tel.: 09131/85-65547
peter.gmeiner@fau.de