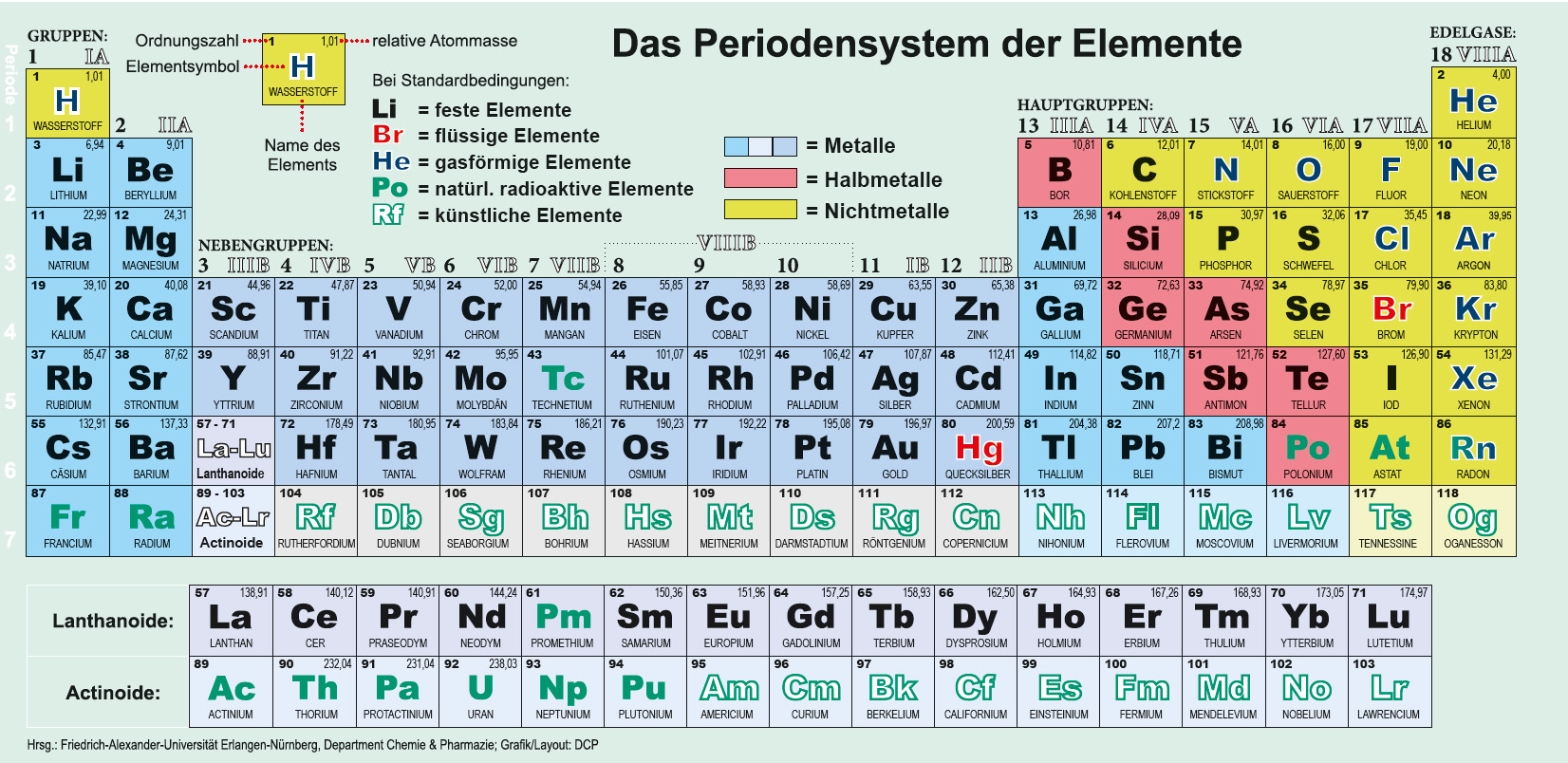
Die Vereinten Nationen haben 2019 zum Internationalen Jahr des Periodensystems erklärt, anlässlich des 150. Geburtstags des Periodensystems. Am 5. Dezember fand hierzu die UN-Abschlussveranstaltung in Tokyo, Japan statt. Die FAU hat zum Jubeljahr des Periodensystems ihre Wissenschaftlerinnen und Wissenschaftler in den vergangenen Monaten zu ihren „Lieblingselementen“ befragt.

„Helium ist nach Wasserstoff das zweithäufigste Element im Universum und macht etwa 25 Prozent der Masse der sichtbaren Materie aus. Das Element ist zum ersten Mal im Sonnenspektrum gefunden worden und heißt deshalb Helium – nach „hélios“, altgriechisch für Sonne.
Helium ist ein Edelgas und spielt nicht nur in der Astronomie eine wichtige Rolle, sondern zum Beispiel auch in der Quantenmechanik, da es das einfachste Mehrelektronenatom ist und Rechnungen zu Atomzuständen ermöglicht.
Es wird auch als Füllgas für Luftballons benutzt und kann für viel Spaß sorgen, da die Stimme nach dem Einatmen von Helium aufgrund der, relativ zur Luft, höheren Schallgeschwindigkeit sehr hoch werden kann.“

„Verbindungen des Berylliums faszinieren auf der einen Seite durch atemberaubende Edelsteine wie Smaragde oder Aquamarine, auf der anderen Seite steht Beryllium im Ruf, das giftigste nicht radioaktive Element zu sein, ob zu Recht ist umstritten.
Beryllium ist aus mehreren Gründen ‚mein‘ Element. Es spielt bei der Elemententstehung in den Sternen eine zentrale Rolle. Wir Menschen nutzten früher berylliumhaltige Edelsteine, sogenannte Berylle als Sehhilfen (daher unser deutsches Wort ‚Brille‘). Heute setzen wir Beryllium und seine Verbindungen im Hightech-Bereich ein; zum Beispiel werden die Spiegel für das James-Webb-Weltraumteleskop daraus gefertigt.
Um das kleinste Metallkation, das wir kennen, passen nur wenige Moleküle – meist vier in tetraedrischer Anordnung. Reaktionen und die zugehörigen Mechanismen an solchen Zentren ebenso wie die Frage, wie sich Berylliumionen in molekularen Käfigen verhalten, stehen im Mittelpunkt meiner Forschung als theoretisch orientierter, in erster Linie anorganischer Chemiker.“

„Ohne Calcium geht nichts! All unsere Sinne funktionieren dank geringster Calciumströme. Neben der Biochemie fasziniert mich die noch junge Organocalciumchemie. Calcium birgt viele Geheimnisse. Kann Calcium Platin ersetzen? Nutzt es d-Orbitale? Die Zukunft ist voller Überraschungen!“
Das FAU-Forschungsteam um Prof. Dr. Harder hat neben anderen Wissenschaftlerinnen und Wissenschaftlern dem Element Calcium durch eine Publikation im interaktiven Periodensystem des Nature-Verlages ein Gesicht gegeben:
https://www.nature.com/immersive/d42859-019-00001-7/index.html

„Aus fachlichem Interesse ist mein Lieblingselement Neodym aus der Gruppe der Seltenen Erden oder Lanthanoiden. Neodym und die anderen Seltenen Erden treten in sehr geringen Konzentrationen in allen Gesteinen der Erdkruste und des Erdmantels auf. Die Messung dieser Elemente hat wesentlich zum Verständnis der chemischen Entwicklung des Planeten Erde und des Sonnensystems beigetragen.
Neodym hat sieben Isotope, von denen zwei (¹⁴²Nd und ¹⁴³Nd) durch radioaktiven Zerfall entstanden sind.
Die Messung dieser Isotope ermöglicht uns Geowissenschaftlern die Altersbestimmung von Gesteinen, die teilweise Milliarden von Jahren alt sind, und Auskünfte über die Bildung des Sonnensystems und der Erde zu geben.
Die Anziehungskraft von Neodym ist inzwischen weit verbreitet, da das Element ein wichtiger Bestandteil der stärksten Magneten ist, die beispielsweise in Elektromotoren verwendet werden.“

„Mein Lieblingselement ist der Phosphor (P) – ein sehr spannendes Element.
Weißen Phosphor möchte man nicht unbedingt in der Hand halten, da man sich dabei im wahrsten Sinne des Wortes die Finger verbrennen könnte.
Umgekehrt wären wir ohne Phosphor aber gar nicht in der Lage, überhaupt irgendetwas in die Hand zu nehmen – es gäbe keinen Bauplan für uns, denn Phosphat ist Bestandteil unseres Erbguts. Zusätzlich würden wichtige Bausteine fehlen, da unser Skelett zum Großteil aus dem Calciumphosphatmineral Hydroxylapatit besteht.
Daher beschäftige ich mich im Rahmen meiner Forschung auch mit Calciumphosphaten für den Einsatz als Knochenersatzstoffe. Phosphor kann also lebensnotwendig oder hochgefährlich sein – auf die Umgebung kommt es an.“

„Sauerstoff fasziniert mich schon seit meiner Schulzeit: die Bindung von Sauerstoff bei Verbrennungsprozessen, die Knallgasreaktion, die zahlreichen farbenfrohen Metalloxide und Mineralien, die Sauerstoffbildung bei der Photosynthese der Pflanzen oder auch der Sauerstoffverbrauch zur Energiegewinnung in der Atmungskette der Zellkraftwerke (Mitochondrien) weckten mein Interesse an diesem Element.
In meiner Forschungstätigkeit als medizinischer Mikrobiologe und Immunologe begegnet mir der Sauerstoff in weiteren, ebenso spannenden Funktionen: Fresszellen benutzen Sauerstoff zur Synthese von Molekülen wie Stickstoffmonoxid, Wasserstoffperoxid oder Hypochlorit, die große Bedeutung für die Infektionsabwehr und die Immunregulation haben.“

„Die Band Nirvana hat einen Song danach benannt, es hilft gegen Depressionen, den Einsatz von Verbrennungsmotoren und führt zu langen Aushärtezeiten von meinem Zement. Lithium wird in der Medizin zur Therapie, in Akkus für E-Autos und als Beschleuniger in Schnellzementen eingesetzt. An Zementen und der Wirkung von Lithium auf ihre Bestandteile forsche ich an der FAU.
Der Name Lithium kommt vom griechischen Wort für Stein, denn daraus wurde es erstmalig gewonnen. Ich habe ein Mineral mitgebracht, das Lithium enthält, manchmal kann man es auch als Schmuckstein kaufen: Es heißt Spodumen. Lithium kann man mit seiner starken roten Flammenfärbung nachweisen.“

„Wasserstoff ist nicht nur der Anfang des Periodensystems, sondern mit weitem Abstand des häufigste Element im Universum: In Massenprozenten bestehen 75 Prozent der Materie im Universum aus Wasserstoff. Die Sterne, die wir am Himmel sehen, erzeugen wie auch unsere Sonne ihre Energie aus der Fusion von Wasserstoff zu Helium. Damit ist Wasserstoff sicherlich auch eines der für uns wichtigsten Elemente.“

„Mein Lieblingselement ist Schwefel (S) – ein facettenreiches Element, das seit über 5000 Jahren bekannt ist.
Beispielsweise nutzten die Ägypter Schwefel zum Bleichen von Textilien, als Arzneimittel und zur Desinfektion. Die alten Griechen schwefelten Wein und Meerrettich zur Verlängerung der Haltbarkeit, und diese Konservierungsmethode wird auch heute noch verwendet.
Im Alten Testament wird Schwefel als Kriegswaffe im Zusammenhang mit der Zerstörung der Städte Sodom und Gomorra erwähnt.
Eine Abhandlung aus der Zeit um 1044 beschreibt Formen des Schwarzpulvers, eine Mischung aus Kaliumnitrat, Holzkohle und Schwefel.
Auch in der Nähe von aktiven Vulkanen kommt Schwefel vor. Die zum Beispiel auf der Insel Vulcano vorhandenen Dampfaustritte stoßen unter anderem Schwefelwasserstoff aus, der an der Austrittstelle kondensiert und gelbe, wunderschön anzuschauende Schwefelkristalle bildet.“

„Mein Lieblingselement ist das Magnesium (Mg), das in zahlreichen Mineralen vorkommt.
Auch mein Hauptforschungsobjekt, die corallinen Rotalgen, bauen es in ihr Kalzitskelett ein – und zwar in Abhängigkeit von den Umweltbedingungen.
Da sie außerdem wie Bäume eine Jahresrhythmik entwickeln, kann ich mit der Magnesiumkonzentration beispielsweise auf frühere Temperaturen oder die voranschreitende Ozeanversauerung schließen – auf das Jahr genau und teils über 100 Jahre in die Vergangenheit.
Das entsprechende Probenmaterial auf dem Meeresgrund der Arktis, meinem Arbeitsgebiet, einzusammeln, ist dabei natürlich eine besondere Freude.“

„Mein Lieblingselement ist der Kohlenstoff (C), das chemische Chamäleon.
Nicht nur, weil ich auf ihm meine wissenschaftliche Karriere aufgebaut habe, sondern auch weil er das wichtigste Element auf der Erde ist.
Ohne Kohlenstoff kein Leben! Mikroorganismen, später Pflanzen und Tiere haben als Biokatalysatoren das CO2 – die einzige Urform von Kohlenstoff auf unserem Planeten – in organische Materie umgewandelt oder in Muscheln biomineralisiert. Daraus sind dann unter anderem Erdöl, Kohle und Kalksteingebirge entstanden, die heute den weitaus größten Teil von C auf der Erde speichern.
Wir Chemiker konnten dann viel später weitere faszinierende C-Formen herstellen, wie die fußballförmigen Fullerene, die Kohlenstoffnanoröhren und das Graphen, das dünnste bekannte Hochleistungsmaterial.“